* 仅供医学专科东说念主士阅读参考开yun体育网

会议速递,紧跟HER2低抒发烧点话题。
导读
HER2低抒发约占总体乳腺癌的45%-55%[1],跟着新式ADC药物在HER2低抒发乳腺癌患者中疗效的开垦,HER2低抒发已成为乳腺癌领域新的靶向颐养亚型,干系进展备受领域学者重心矜恤。2024年欧洲内科学会亚洲年会(ESMO Asia)于当地时辰12月6日-8日在新加坡普遍召开。本次大会上,HER2低抒发乳腺癌领域的多项计划着力重磅揭晓。为更好传递大会前沿信息,医学界肿瘤频说念特邀中山大学孙逸仙牵挂病院丁林潇潇陶冶针对部分计划进行长远解读,并发表蹙迫不雅点。
37MO - HER2低抒发异质性过火对转化性乳腺癌中T-DXd疗效的影响
■计划布景
T-DXd已获批用于HER2低抒发转化性乳腺癌患者。在归并患者中,原发灶和转化灶之间HER2景色可能存在不一致性。当今对于使用哪种标蓝本细目HER2景色以指引T-DXd颐养,仍存在争议[2]。
■计划武艺
本计划计较纳入2156例HER2景色在原发灶过火匹配的转化灶中均可评估的乳腺癌患者,以评估HER2抒发的不一致性。其中165名接纳T-DXd颐养的患者根据其原发灶和转化灶的HER2抒发水平分为三个部队:部队1包括原发灶和转化灶均为HER2阳性或低抒发的患者;部队2包括原发灶为HER2阳性或低抒发,而转化灶改换为HER2 0抒发的患者;部队3则包括原发灶为HER2 0抒发,但转化灶改换为HER2阳性或低抒发的患者。计划主要至极包括无进展生涯期(PFS)、总生涯期(OS)、客不雅缓解率(ORR)、疾病狂放率(DCR)和临床获益率(CBR)。
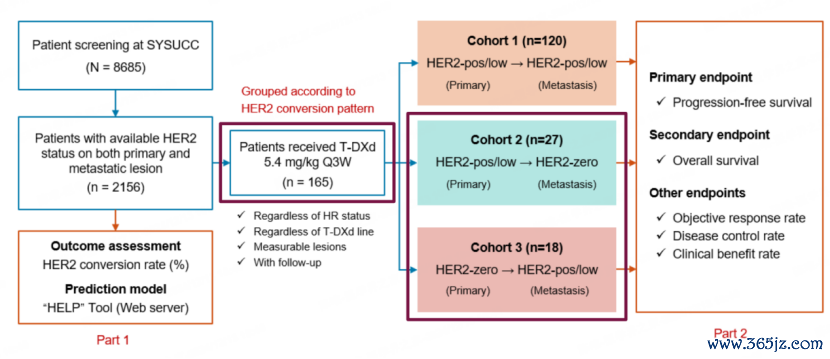
图1. 计划计划和HER2改换形式
■计划末端
在原发灶和匹配的转化灶之间,HER2抒发的不一致率高达25.5%,这一表象与病理组织学分级、激素受体景色、转化部位和转化时辰等颓败风险身分干系。计划者开垦了HER2低抒发不一致性的展望(HeLP)器用(https://helptool.shinyapps.io/dynnomapp/),该器用大要利用原发灶肿瘤的信息,准确展望转化灶的HER2抒发景色(AUC=0.82)。在接纳T-DXd颐养的患者中,部队1和部队3的ORR区分为65.8%和72.2%,权贵高于部队2(37.0%)。此外,部队1和部队3在PFS和OS方面也展现出更优的末端,其中部队1的中位PFS为17.0个月,中位OS为34.1个月;部队3的中位PFS为17.2个月,中位OS尚未达到。比较之下,部队2的中位PFS为7.7个月,中位OS为18.5个月。
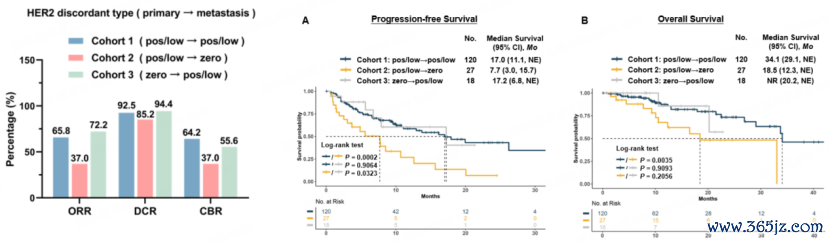
图2. 不同HER2改换形式中患者接纳T-DXd颐养的疗效数据
■计划论断
与原发灶肿瘤标本比较,转化灶中的HER2抒发水平能更准确地展望T-DXd颐养的疗效。因此,提出在晚期乳腺癌患者中再行评估转化灶的HER2景色,以便在制定T-DXd颐养决策时作念出更理智的采用。
■计划点评
丁林潇潇
由于乳腺癌HER2异质性的存在,HER2抒发景色在原发灶和转化灶之间可能存在相反,尤其HER2低抒发乳腺癌存在高度的时空异质性,这在既往多项计划中一经得到了阐明。DB04计划针对不相似本类型进行的亚组分析标明[3],岂论样蓝本源是原发灶如故转化灶,惟一患者检测为HER2低抒发,王人能从T-DXd颐养中权贵获益。这标明T-DXd的疗效似乎不受HER2异质性的影响。DB06计划标明,经当地实验室检测为IHC 0的患者中,64%经中心实验室检测为HER2低抒发或HER2超低抒发,赢得接纳T-DXd颐养的契机[4]。勾搭本项计划着力,尽管转化灶检测为HER2低抒发的部队与原发灶检测为HER2低抒发的部队从T-DXd颐养中的获益存在一定相反,但是惟一该病例原发灶或转化灶任何点检测为HER2低抒发,王人能算作T-DXd的获益上风东说念主群。这些共同强调了针对转化灶,尤其是原发灶为HER2 0的病例再次活检的蹙迫性[5-8],这小数也在本计划中得到了充分考据。
同期这项计划也给到临床一定启示,尽管原发灶和转化灶的HER2低抒发景色王人能请示临床用药,但是在在临床施行中,医师可能会根据患者的具体情况和颐养需求,采用检测原发灶、转化灶或两者的HER2抒发景色,以赢得最全面和最干系的颐养信息。
52P - T-DXd在多线经治HER2低抒发转化性乳腺癌中的确切全国疗效和安全性:来自中国东说念主群的凭据
■计划布景
对于T-DXd颐养HER2低抒发转化性乳腺癌,当今莫得确切全国数据来评估免疫组织化学(IHC)1+和2+亚组之间的疗效相反。因此,本计划拜谒了T-DXd在中国确切全国HER2低抒发转化性乳腺癌患者中的灵验性和安全性,并比较了这两个类别的末端 [9] 。
■计划武艺
这项单中心、挂念性计划招募了在2022年6月至2023年12月技艺接纳T-DXd颐养的HER2低抒发转化性乳腺癌患者。主要计划至极是PFS。还陈诉了ORR和CBR。通过记载不良事件(AEs)来监测安全性。
■计划末端
在70名安妥条目的患者中,37名(52.9%)为IHC 1+,33名(47.1%)为IHC 2+。33名(47.1%)患者在T-DXd颐养前接纳了≥3线化疗。T-DXd的中位驱动剂量为4.6 mg/kg,每三周一次。IHC 1+和2+亚组的中位PFS区分为3个月和5个月(HR=0.51, 95%CI: 0.28-0.95, p=0.034)。ORR区分为16.2%和27.3%,而CBR区分为24.3%和36.4%。接纳≥3线既往化疗的患者与接纳≤2线的患者比较,中位PFS更短(3个月 vs 5个月,更正后HR=1.99,95%CI:1.10-3.58,p=0.022)。接纳T-DXd较高驱动剂量的患者比接纳较低剂量的患者预后更好(更正后HR=0.64,95%CI:0.45-0.89,p=0.009)。恶心是最常见的AEs,发生在30名(42.9%)参与者中,而最常见的3-4级AEs是中性粒细胞减少症、贫血和白细胞减少症(各7.1%)。在IHC 1+和2+亚组之间未不雅察到毒性方面的权贵相反。
■计划论断
与IHC 1+患者比较,IHC 2+患者更有可能从T-DXd颐养中获益。既往多线化疗和驱动剂量不及可能会对T-DXd的疗效产生负面影响。
■计划点评
丁林潇潇
既往DAISY计划[10]标明T-DXd在不同HER2抒发水平(HER2过抒发、HER2低抒发、HER2 0抒发)晚期乳腺癌患者中均灵验,请示HER2抒发水平可能算作T-DXd疗效展望的生物秀气物。但在HER2低抒发乳腺癌部队中,IHC 1+和IHC 2+/ISH-亚组患者的中位PFS(6.9个月 vs 5.8个月)和ORR(39.0% vs 35.5%)获益相似。此外,DB04计划[11]亚组分析不雅察到相似的趋势,两个亚组的中位PFS区分为10.3个月和10.1个月。这些似乎共同标明HER2低抒发界说中的IHC评分并不影响T-DXd的疗效。可是,意念念的是,DB06计划[12]标明,在接纳T-DXd颐养的HER2低抒发晚期乳腺癌患者中,IHC 1+和IHC 2+/ISH-亚组的中位PFS区分为12.9个月和15.2个月,二者似乎存在一定的相反。
本项计划中,IHC 1+患者比较IHC 2+/ISH-患者的获益似乎更差,在确切全国角度揭示了HER2低抒发晚期乳腺癌中不同IHC评分景色患者从T-DXd颐养中的获益情况,具有一定临床参考价值。与此同期,接头到DB06计划[12]阐明了HER2超低抒发(IHC 0-1+)患者与HER2低抒发患者从T-DXd颐养中的获益一致,中位PFS均为13.2个月。这不仅再次激勉了临床上对于HER2低抒发下限的科学念念考,而且也请示翌日HER2 IHC评分在传统HER2阴性乳腺癌中的展望价值还需要更多的计划来进一步探索和考据。
另一方面,该计划标明既往化疗经治线数越少,患者从T-DXd颐养中的获益越多。这与DB04和DB06计划中HR+/HER2低抒发晚期乳腺癌患者呈现出的获益趋势一致,在DB04计划中T-DXd针对既往接纳过1-2线晚期化疗患者的中位PFS为10.1个月[11]。DB06计划中,T-DXd针对既往未接纳过化疗患者的中位PFS为13.2个月[12],这些共同考据了T-DXd在HR+/HER2低抒发晚期乳腺癌中更早线用药的获益上风。此外,该计划还揭示,在临床施行中,T-DXd应该足剂量用药,才智最大化患者获益。
总之,这项确切全国计划反应了中国HER2低抒发晚期乳腺癌患者应用T-DXd的灵验性和安全性,跟着T-DXd在中国临床的日益陶冶,该计划对于优化T-DXd的临床用药具有蹙迫真谛。
41P - HER2低抒发和HER2 0抒发景色对一线使用芳醇化酶扼制剂±CDK4/6扼制剂颐养的转化性HR阳性乳腺癌患者的影响:一项多中心挂念性分析
■计划布景
HER2低抒发景色是HR阳性转化性乳腺癌中强效抗HER2颐养的展望身分。可是,HER2低抒发景色对内分泌颐养的影响仍不明晰。本计划旨在探索HER2低抒发和HER2 0抒发对于HR阳性转化性乳腺癌患者一线使用芳醇化酶扼制剂(AI)±CDK4/6扼制剂(CDK4/6i)的疗效影响 [13] 。
■计划武艺
本计划挂念性审查了2017年至2022年技艺,在泰国六所三级病院接纳一线AI±CDK4/6i颐养的HR阳性转化性乳腺癌患者,包括绝经后以及接纳卵巢功能扼制颐养的绝经前患者。计划通过比较未更正和更正基线特征(包括年齿、ECOG、新发转化、颐养无进展间期、内脏转化和转化部位数目)后的PFS和OS,并利用褂讪逆概率颐养加权(sIPTW)武艺进行更正,以评估颐养效果。
■计划末端
在504名患者中,219名(43.5%)发扬为HER2低抒发,285名(56.5%)发扬为HER2 0抒发。HER2低抒发乳腺癌患者的中位会诊年齿为60岁,而HER2 0抒发患者为61岁。在HER2低抒发和HER2 0抒发患者中,区分有52.5%和43.9%接纳了CDK4/6i集会AI颐养。其中72%的患者接纳了瑞波西利颐养,28%接纳了哌柏西利颐养。CDK4/6i集会AI颐养的中位随访时辰为29个月,而单独AI颐养的中位随访时辰为35个月。计划数据截止至2023年9月30日。
在HER2低抒发和HER2 0抒发HR阳性转化性乳腺癌患者中,CDK4/6i集会AI颐养与单独AI颐养比较,败闪现更优的颐养效果。其中HER2低抒发组中,CDK4/6i集会AI颐养的中位PFS为25.5个月,而单独AI颐养为18个月,中位OS区分为52.4个月和37.9个月。HER2 0抒发组中,CDK4/6i集会AI颐养的中位PFS为25.5个月,单独AI颐养为12.8个月,中位OS区分为45.9个月和38.4个月。
表1. HR阳性、HER2低抒发和HER2 0抒发患者中,CDK4/6i比较AI的疗效
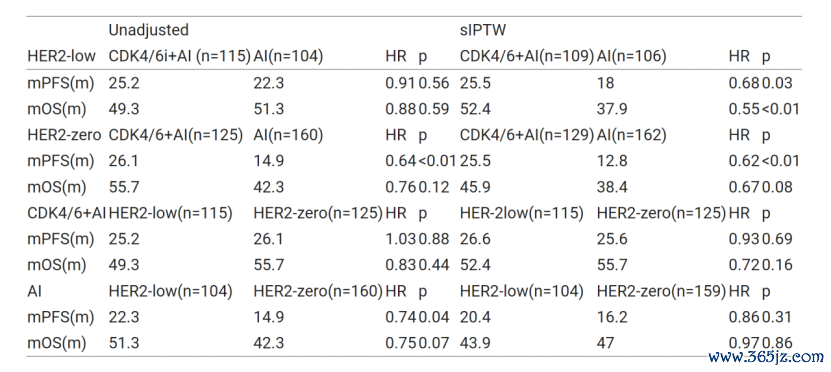
■计划论断
岂论在HER2低抒发如故HER2 0抒发的HR阳性转化性乳腺癌患者中,CDK4/6i集会AI颐养比较单独AI颐养,能带来更权贵的生涯获益。此外,HER2低抒发景色本人并不影响患者接纳CDK4/6i集会AI颐养或单独AI颐养的预后。这一发现对于指引临床颐养决策具有蹙迫真谛,相配是在采用最好颐养决策时。
■计划点评
丁林潇潇
由于HR和HER2通路之间存在交叉串扰,针对HR通路的颐养连接会引起HER2通路的上调,从而导致内分泌耐药的发生[14]。这一发现激勉了临床上对于HER2抒发水平能否算作HR+/HER2-乳腺癌预后和展望办法的长远念念考。在HR阳性乳腺癌患者中,HER2低抒发患者约莫占55%至65%[1]。对于HR+/HER2低抒发晚期乳腺癌患者,一线首选CDK4/6i集会内分泌颐养。
对于HER2低抒发是否影响HR阳性患者从CDK4/6i集会内分泌一线颐养中获益的问题,当今仍存在争议。一些纳入CDK4/6i经治HR阳性转化性乳腺癌患者的挂念性分析标明,HER2低抒发患者的预后可能比HER2 0抒发患者更差。可是,也有计划败露这两类患者的预后相似[14],包括本计划在内,并未阐明HER2低抒发会对患者接纳CDK4/6i集会内分泌颐养的疗效产生影响。总之,该计划为进一步探讨HER2低抒发在HR阳性乳腺癌中的预后价值提供了新的凭据救助。但尽管如斯,HER2低抒发景色对内分泌颐养是否存在影响,翌日仍需更多计划的长远探索和考据。
论断
总之,HER2低抒发已成为刻下乳腺癌领域的诊疗热门,上述计划涵盖了其预后价值、颐养决策以及病观点诊等方面试验,为临床提供了蹙迫参考。 投诚翌日跟着更多计划的长远探索,HER2低抒发乳腺癌的诊疗将会开启新的篇章,为更多患者带来福音。
内行简介

丁林潇潇
中山大学孙逸仙牵挂病院乳腺肿瘤内科副主任医师,博士
广东省老年保健协会乳腺癌整合颐养专科委员会副主委兼文书长
广东省医疗行业协会乳腺内科责罚分会副主委
主要计划标的:乳腺癌内科颐养
以第一或共同第一作家身份在《Advance Science》、《Cell Reports》等杂志发表著作,主抓1项国当然后生基金,参与多项临床计划
精彩资讯等你来
参考文件:
[1]《东说念主2低抒发乳腺癌临床诊疗共鸣(2022版)》
[2]Zou YT, Deng XP, Xie JD, et al. HER2-low heterogeneity and its impact on benefit from trastuzumab deruxtecan in metastatic breast cancer. 2024 ESMO Asia. 37MO.
[3]Prat A, Modi S, Tsurutani JJ, et al. Determination of HER2-low status in tumors of patients with unresectable and/or metastatic breast cancer in DESTINY-Breast04. 2022 SABCS. HER2-18.
[4]Salgado RF, Bardia A, Curigliano G,et al. HER2-low and HER2-ultralow status determination in tumors of patients with hormone receptor–positive metastatic breast cancer in DESTINY-Breast06. 2024 ESMO. LBA21.
[5]Tarantino P, Viale G, Press MF, et al. ESMO Expert Consensus Statements (ECS) on the definition, diagnosis, and management of HER2-low breast cancer. Ann Oncol. 2023 Jun 1:S0923-7534(23)00693-2.
[6]Wolff AC, Somerfield MR, Dowsett M, et al. Human Epidermal Growth Factor Receptor 2 Testing in Breast Cancer: ASCO-College of American Pathologists Guideline Update. J Clin Oncol. 2023 Aug 1;41(22):3867-3872.
[7]Gennari A, André F, Barrios CH, et al. ESMO Clinical Practice Guideline for the diagnosis, staging and treatment of patients with metastatic breast cancer. Ann Oncol. 2021 Dec;32(12):1475-1495.
[8]《乳腺癌HER2检测指南(2024版)》
[9]Wu S, Li JB, Bian L, et al. Real-world efficacy and safety of trastuzumab deruxtecan in heavily pre-treated HER2-low metastatic breast cancer with distinct IHC statuses: Evidence from a Chinese population. 2024 ESMO Asia. 52P.
[10]Mosele F, Deluche E, Lusque A, et al. Trastuzumab deruxtecan in metastatic breast cancer with variable HER2 expression: the phase 2 DAISY trial. Nat Med. 2023 Jul 24.
[11]Modi S, Jacot W, Yamashita T, et al. DESTINY-Breast04 Trial Investigators. Trastuzumab Deruxtecan in Previously Treated HER2-Low Advanced Breast Cancer. N Engl J Med. 2022 Jul 7;387(1):9-20.
[12]Bardia A, Hu X, Dent R, et al. DESTINY-Breast06 Trial Investigators. Trastuzumab Deruxtecan after Endocrine Therapy in Metastatic Breast Cancer. N Engl J Med. 2024 Sep 15.
[13]Susiriwatananont T, Wongkraisri C, Dajsakdipon T, et al. Impact of HER2-low and HER2-zero status on metastatic hormonal receptor-positive breast cancer patients treated with first-line aromatase inhibitors, with or without CDK4/6 inhibitors: A multicenter retrospective analysis. 2024 ESMO Asia. 41P.
[14]Önder T, Ateş Ö, Öner I, et al. Relationship between HER2-low status and efficacy of CDK4/6 inhibitors in advanced breast cancer: a real-world study. Int J Clin Oncol. 2024 Jul;29(7):972-984.
* 此文仅用于向医学东说念主士提供科学信息,不代表本平台不雅点